Ácido sulfúrico H2SO4
Antes de empezar con esta publicación quiero dejar en claro que la última forma no la he puesto en práctica y no podría asegurar que funciona al 100%, aún así le invito a intentarlo.
Primer forma: Fallido
Este fue mi primer intento de sintetizar ácido sulfúrico. Quiero agregar este procedimiento ya que es una de las tantas muestras que la prueba y el error son parte del camino. Por eso mismo agregué una sección para mencionar cada fallo que visto.
PRECAUCIONES
- En la reacción se sintetiza un gas que puede molestar a los ojos y si se inhala puede formar ácidos dentro del sistema respiratorio.
- En la última forma se trata con un sistema aislado, la acumulación de presión al momento de formar el gas SO
2 puede llegar a reventar el sistema causando daños por quemaduras químicas
MATERIALES
- Azufre
- Peróxido de hidrógeno (H2O2)
- Vasos para pesar
- Tapa
- Báscula
ECUACIÓN
S(s)+H2O2(l)→SO2(g)+H2O(l)
PROCEDIMIENTO
- Pesar una cantidad de peróxido de hidrógeno
- Pesar una parte proporcional de azufre conforme al peróxido de hidrógeno
- Agregar ambos reactivos y tapar
- Esperar la formación del dióxido de azufre
PROCEDIMIENTO DETALLADO
Tener en cuenta la siguiente proporción: por cada gramo de peróxido de hidrógeno habrán 0.03g de azufre
- 1gH2O2/0.03gS
- 1mlH2O2/0.0012gS
- Pesar una cantidad de peróxido de hidrógeno y calcular así la cantidad necesaria de azufre
- Pesar una parte proporcional de azufre conforme al peróxido de hidrógeno
- Agregar ambos reactivos y tapar (de preferencia en un vaso de precipitado)
- Esperar la formación del dióxido de azufre
No se forma el compuesto que se quiere sintetizar (H2SO4)
EXPERIMENTO FALLIDO: FALLOS Y OBSERVACIONES
- No se forma ninguna liberación de gas; por lo tanto no se obtuvo el gas (SO2)
- La mezcla de agua con azufre forma una especia de repulsión
- El azufre no se puede disolver en temperaturas ambiente ni con el calor de una vela
- La solución obtenida no reacciona con bases; por lo tanto no se puede tener ácido en la muestra (prueba de bicarbonato sódico viejo con grupos pero sin impurezas)
Segunda forma: Correcto
Esta forma ha sido inspirada en un video que forma parte del canal de The Sience Furry
Así mismo me gustaría aclarar que el procedimiento será muy sencillo en donde se utilizarán materiales que la mayoría de personas tiene en casa
MATERIALES
- Lata de refresco
- Boca de botella
- Botella de plástico de preferencia ya que se podra notar el aumento en presión
- Manguera (puede ser de algún atomizador)
- Fuente de calor
- Peróxido de hidrógeno
- Azufre
En caso de notar un pequeño aumento en la presión destapar lentamente
SISTEMA
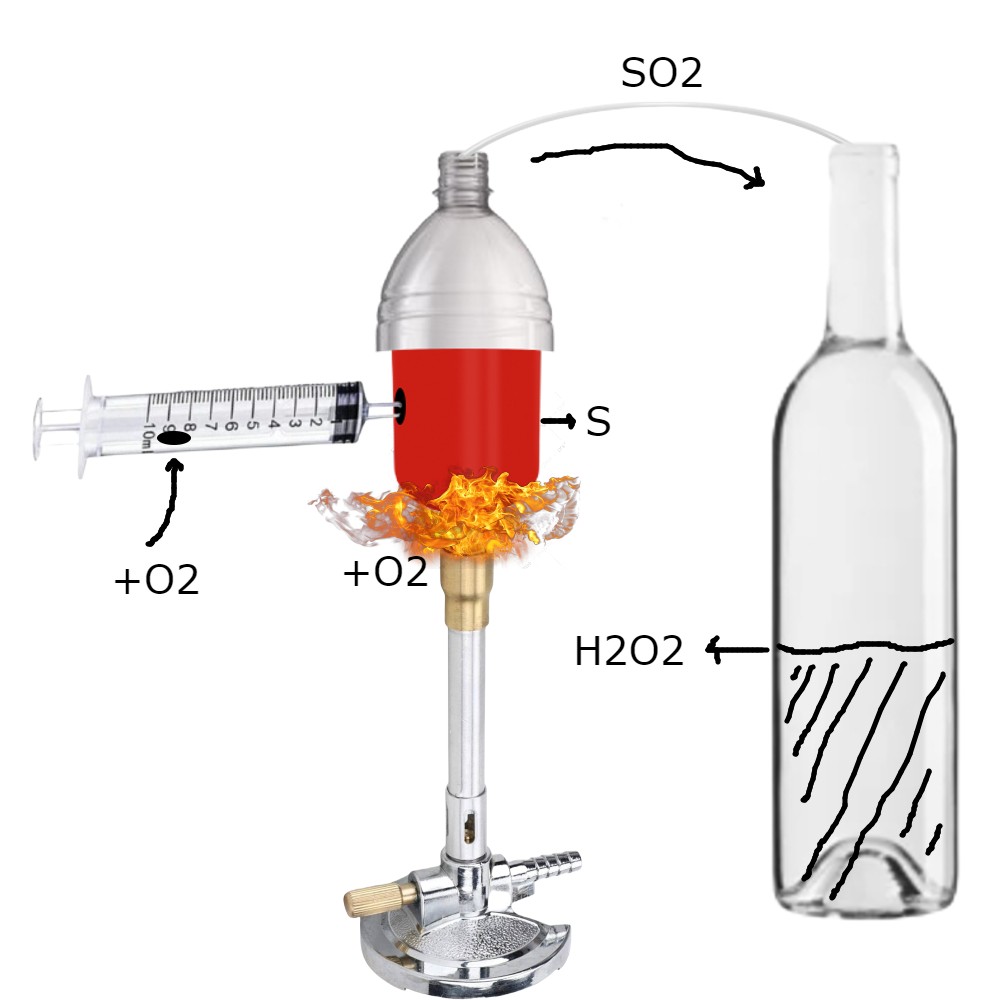
- Hacer un hueco a la jeringa en el tercer cuartil
- hacer un hueco a la lata
- Cortar la parte superior de la lata
- Cortar la botella
- Hacer huecos a las tapas
- Aislar el sistema con cinta
ESTEQUIMETRÍA
Recomiendo leer el anterior apartado de procedimiento detallado
PROCEDIMIENTO
- Armar el sistema
- Colocar el azufre en la lata
- Combustionar el azufre
- Esperar a que la botella del peróxido de hidrógeno se llene de humo y entonces desconectar. Dentro de este paso el oxígeno que alimenta la combustión se consumirá y dejará de quemarse, esto interrumpirá la reacción de S + O2→SO2, para eso tendrás que meter oxígeno con la jeringa
- Tapar y agitar durante 2 segundos
en caso de que la mecánica con la jeringa no sirva recomiendo desconectar el sistema de la parte de la lata y de la parte del peróxido, de esta forma podrás agitar y mezclar y hacer reaccionar SO2+H2O2 →H2SO2 y se llenará de oxígeno otra vez el sistema. Dejo al criterio de cada uno su forma de solucionar el problema, si gusta me lo puede comentar en mi contacto y lo publico con su debida citación